热休克蛋白的特点 热休克蛋白的功能介绍
热休克蛋白 Heat Shock Proteins (HSPs),是在从细菌到哺乳动物中广泛存在一类热应急蛋白质。当有机体暴露于高温的时候,就会由热激发合成此种蛋白,来保护有机体自身。许多热休克蛋白具有分子伴侣活性。按照蛋白的大小,热休克蛋白共分为五类,分别为HSP100,HSP90,HSP70,HSP60 以及小分子热休克蛋白 small Heat Shock Proteins (sHSPs)( Kyeong et al., 1998)。 分布
小分子热休克蛋白分子量为12-34KD,它的分布极为广泛,从细菌到人的基因组里都有小分子热休克蛋白的基因。
与其他大分子的热休克蛋白不同的是,小分子热休克蛋白似乎对于细胞的功能并不是必不可少的。但是,sHSPs具有多种功能,包括赋予细胞以耐热性以抵抗高温,作为分子伴侣以防止蛋白聚集,对抗正常的细胞死亡,从而调节细胞的生存和死亡的平衡。能避免底物变性的sHSPs最少量与底物和热休克蛋白都有关(Rosalind et al., 1998)。
表现
许多小分子热休克蛋白基因一般并不表达,显著表达小分子热休克蛋白一般是细胞受到外部刺激的时候,比如高温刺激。现已发现,除了热刺激之外还有许多物理、化学刺激可以激活小分子热休克蛋白的表达,例如紫外线、射线、机械损伤、酸、氧化剂等等。可见,小分子热休克蛋白是抵御外界不良刺激的重要物质。当将生物的整体、组织、细胞等从其生活的温度范围内急剧地从低温移向高温时,可显著地降低一些蛋白质的合成。例如将果蝇的幼虫或培养细胞从28℃移至35℃时,则几乎大部分的蛋白质合成停止;与此相反,而休克蛋白的合成却反而被促进。这种促进作用主要是在信使RNA的合成(转录)阶段产生的。同样的现象也见于哺乳类动物、培养细胞、原生动物、植物组织和细菌等。另外观察到,由休克以外的其他处理也会发生类似的现象。这种现象的生理意义尚不清楚,但推测是与生物的温度适应现象有关系。
特点
HSP在生物界中的一个重要特点是它们在进化过程中的高度保守性。例如。从大肠杆菌、酵母、果蝇和人体分离的分子量为70kD的HSP,如果对它们进行全氨基酸序列分析,就可发现它们具有80%以上的相似性。HSP在进化过程中的高度保守性,说明它们具有普遍存在的重要生理功能。然而在这方面的研究,迄今还很不充分。 功能
HSP可提高细胞的应激能力,特别是耐热能力。预先给生物以非致死性的热剌激,可以加强生物对第二次热剌激的抵抗力,提高生物对致死性热剌激的存活率,这种现象称为热耐受。对此现象的分子机制仍不太清楚,但许多研究均发现了HSP的生成量与热耐受呈正相关。
HSP还可调节Na+-K+-ATP酶的活性。某些细胞经热休克丧失的Na+-K+-ATP酶活性可在3℃培养中随着HSP的产生而得到部分恢复。HSP的诱导剂亚砷酸钠亦可使Na+-K+-ATP酶的活性升高。这种现象可被放线菌素D和环已酰亚胺抑制,提示Na+-K+-ATP酶活性升高是一种基因表达的结果,而不是亚砷酸钠直接作用的结果。
有人通过四膜虫属细胞热休克的研究,发现有些HSP具有促进细胞内糖原异生和糖原生成的作用,使细胞内糖原贮量增多,从而提高应激能力。
此外,有人还报道,热、乙醇、亚砷酸钠的预处理不仅能使某些细胞产生热耐受,还能使细胞对阿霉素(adriamycin)的耐受性增强,提示HSP可以增强对各种损伤的抵抗力。
至于在人类的应激中,HSP究竟起什么作用,还知之甚少。
热休克蛋白是生物体内最古老的分子之一,是一种保护性蛋白,受到高温等恶劣环境袭击时,就会被大量合成(正常情 况下也有少许存在),从而帮助每个细胞维持正常的生理活动,阻止影响细胞健康的蛋白质相互作用,促进有利于健康的相互作用。如此,不同蛋白质间就形成了稳 定而有效的联系机制,极端条件对人体损害就大为减轻。
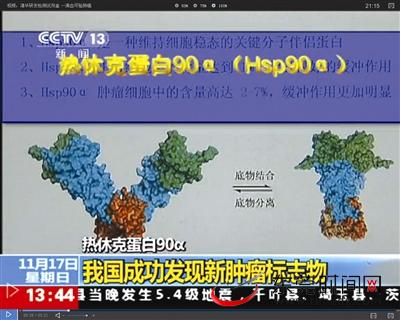
热休克蛋白能与很多蛋白质分子结合,发挥多种生理功能:帮助氨基酸链折叠成正确的三维结构,清除受损而无法正确折叠的氨基酸链,护送蛋白分子寻找目标分子以免受到其它分子的干扰等。
热休克蛋白不仅会保护对于基本生理过程中不可或缺的蛋白,还会分解受损蛋白,回收合成蛋白的原材料,让细胞内的生理化过程得以平稳运行。因此,当细胞受到很大环境压力时,它的第一反应就是合成更多的热休克蛋白。