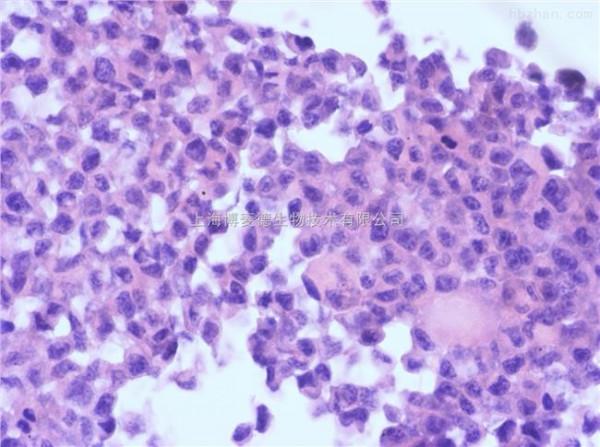
了解恶性肿瘤发生浸润和转移的机制 防止疾病的感染
恶性肿瘤的浸润和转移机制
(1)局部浸润:恶性肿瘤局部浸润的机制目前尚未十分明了,但已知是一个由一系列步骤组成的复杂过程。前面提到的浸润能力强的瘤细胞亚克隆的出现和肿瘤血管形成对此都起着重要的作用。
正常上皮细胞之间有各种细胞粘附分子(cell adhesion molecules,CAMs)如上皮粘连素(E—cadherin)将其彼此胶着在一起,不能单独分离。若将编码上皮粘连素DNA插入到瘤细胞基因组中,则可使其丧失转移和浸润能力 。瘤细胞彼此分散才能侵入细胞外基质(extracellular matrix,ECM)。细胞外基质在机体内分隔上皮组织和结缔组织,包括基底膜和间质性结缔组织,主要是由胶原、糖蛋白和蛋白多糖组成。正常上皮细胞与基质的结合是通过存在于上皮细胞膜表面的整合素(integrin)的粘附分子与存在于基质中的其配体的结合来实现的。
癌细胞的ECM主要成成分——基底膜的侵袭是一主动过程,可分为四个步骤:
1肿瘤细胞彼此之间的粘附力减少(detachment):局部发生浸润时,第一步是由细胞粘附分子介导的肿瘤细胞彼此之间的粘附力减少,而癌细胞与基质的附着力增加。
2癌细胞附着于基底膜(attachment):正常上皮细胞具有的一种整合素——层粘连蛋白(laminin,LN)的受体,只分布在细胞的基底面,能与基底膜的LN分子结合而使上皮细胞附着。而癌细胞则有更多的LN受体,分布于癌细胞的整个表面,使癌细胞更容易与基底膜粘附。例如已发现,人的侵润性乳腺癌细胞与LN的结合能力为正常或良性乳腺上皮细胞的50倍,这类病人发生淋巴结转移的机会大大高于LN受体较少的乳腺癌病人。纤维粘连蛋白(fibronectin,FN)也是基底膜的成分,可与上皮细胞表面的一种整合素——FN受体结合而使细胞附着于基底膜。癌细胞FN受体表达增加和其侵袭性之间也存在于与LN类似的关系;除此之外癌细胞还可以表达多种整合素作为细胞外基质的受体,如胶原和vicronectin的受体。
3细胞外基质的降解(degradation);在癌细胞与基底膜紧密接触4~8小时后,ECM的成分,如LN、FN、蛋白多糖和胶原纤维(Ⅳ型)可被癌细胞直接分泌的蛋白溶解酶(包括Ⅳ型胶原酶、尿激酶型胞浆素原活化物、组织蛋白酶D等)溶解,使基底膜产生局部的缺损。癌细胞也可诱导宿主细胞(如纤维母细胞)产生蛋白酶,使ECM溶解。Ⅳ型胶原酶是一种金属蛋白酶,能分解上皮和血管基底膜的Ⅳ型胶原纤维,已有报告指出在乳腺癌和胃癌细胞有这种酶的过度表达。动物实验还发现Ⅳ型胶原酶的抑制剂可以大大减少转移的发生;
4癌细胞的移出(migration);癌细胞通过被溶解的基底膜缺损处游出是借助于自身的阿米巴运动。近来发现肿瘤细胞的衍生的细胞激肽,如自分泌移动因子(autocrine motility factor),如肝细胞生长因子和胸腺素β15(thymosin β15)可介导瘤细胞的移动。基质成分(如胶原、蛋白多糖)的降解产物和某些生长因子(如胰岛素样生长因子Ⅰ和Ⅱ)对癌细胞有化学趋向性,还可以促进血管形成和肿瘤生长。癌细胞穿过基底膜后,重复上述步骤进一步溶解间质性的结缔组织,在间质中移动。到达血管壁时,可以以同样方式穿过血管的基底膜进入血管。
(2)血行播散:进入血管的癌细胞形成新的转移灶的可能性小于千分之一,因单个癌细胞进入血管后绝大多数为机体的免疫细胞(NK)消灭。但被血小板凝集成团的癌细胞形成的瘤栓则不易被消灭,并可与形成栓塞处的血管内皮细胞粘附,然后以前述机制穿过血管内皮和基底膜,形成新的转移灶。由于肿瘤的异质化而选择出的高侵袭性的瘤细胞亚克隆,尤其容易形成广泛的血行播散。新近发现一种称为CD44的粘附分子可能与血行播散有关。在正常的T细胞表面的CD44分子可以通过识别毛细血管后静脉内皮上的透明质酸而回到特定的淋巴组织。而在结肠癌CD44的变异型(如V6)的高表达提示高转移。
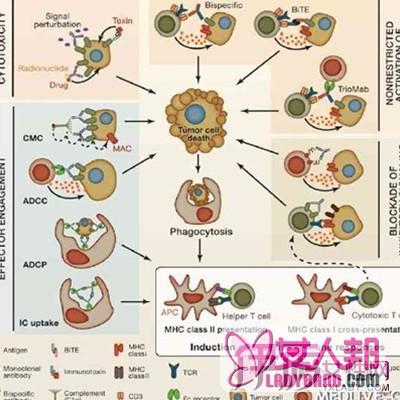
恶性肿瘤细胞侵出基底膜进入细胞外间质,侵入血管并形成新的转移灶
转移的发生不是随机的。早在1889年Paget在对700多侧乳腺癌的转移进行分析后,就发现有明显的器官倾向性,并提出有名的“种子和土壤”学说。血行转移的位置和器官分布,在某些肿瘤具有特殊的亲和性,如肺癌易转移到肾上腺和脑;甲状腺癌、肾癌和前列腺癌易转移到骨;乳腺癌常转移到肺、肝、骨、卵巢和肾上腺等。产生这种现象的原因还不清楚,可能是由于这些器官的血管内皮上有能与进入血循环的癌细胞表面的粘附分子特异性结合的配体(如血管细胞粘附分子),或者由于靶器官能够释放某些吸引癌细胞的化学吸引物质(如胰岛素样生长因子Ⅰ和Ⅱ)。此外,转移瘤在某些组织或器官中不易形成,也可能与这些器官或组织的环境不适合肿瘤的生长有关。如脾虽然血液循环丰富但转移癌少见,可能是因为脾是免疫器官;横纹肌转移瘤很少,可能是因为肌肉经常收缩使瘤细胞不易停留或肌肉内乳酸含量过高,不利于肿瘤生长。
(3)肿瘤转移的分子遗传学:目前尚发现一个单独的转移基因,但已发现一种肿瘤抑制基因——nm23的表达水平与肿瘤的侵袭和转移能力之间存在有意义的关系。在小鼠模型中,nm23的表达高者具有低转移性;nm23表达低10倍者伴有高转移。人类的nm23基因定位于第17位号染色体。在侵袭性强的肿瘤中nm23基因丢失。临床上对人乳腺癌的观察发现,淋巴结转移少于三个者,nm23蛋白表达水平高;而有广泛转移者nm23蛋白表达的水平一般均低。如能将nm23蛋白作为标记物来预测转移并且在治疗上用于抑制转移,将是肿瘤治疗的一个突破。现此问题正在积极研究中。