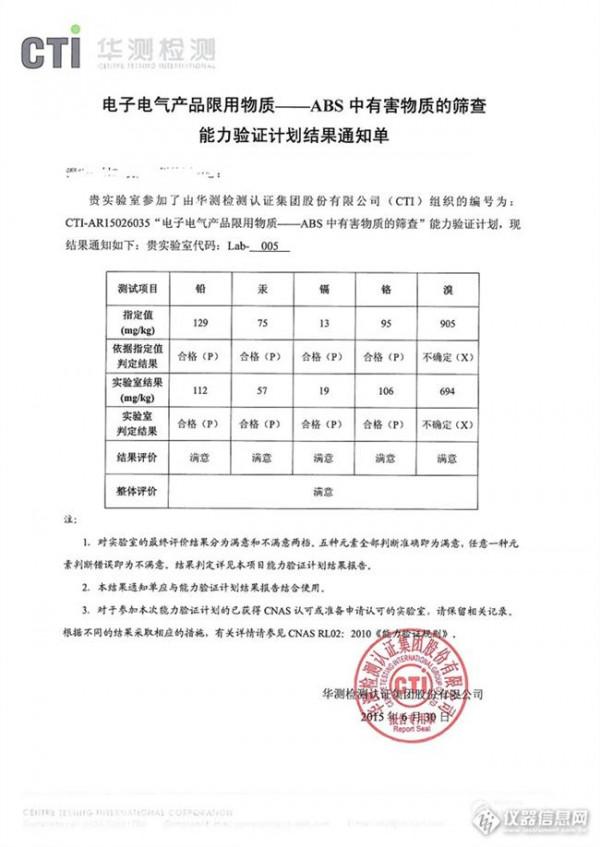
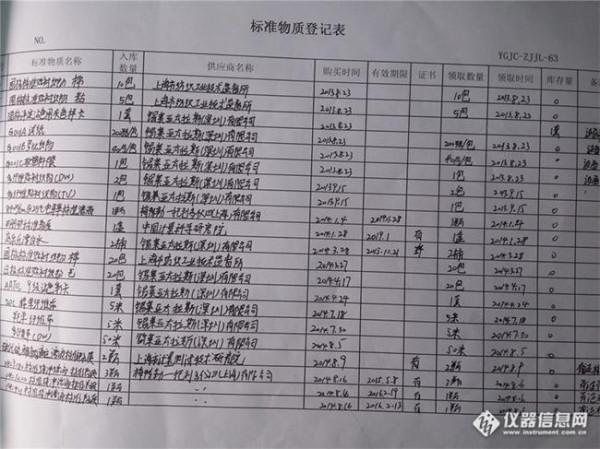
黄晓龙的签名 有关物质分析方法验证的可接受标准简介黄晓龙
国家食品药品监督管理局药品审评中心-电子刊物 发布日期 20060208 栏目 化药药物评价>>化药质量控制 标题 有关物质分析方法验证的可接受标准简介 作者 黄晓龙 部门
正文内容 黄晓龙 摘要: 本文介绍了在对有关物质检查所用的分析方法进行方法学验证时, 各项指标的可 接受标准,以利于判断该分析方法的可行性。 关键词:有关物质检查 分析方法验证 可接收标准 药品中的有关物质泛指在药品的生产与储存过程中产生的工艺杂质或降解产物。
由于这 些有关物质的存在会影响到药品的纯度, 进而可能会产生毒副作用, 所以有关物质的控制是 药品研发的一个重要方面, 也是我们在药品审评中一直重点关注的要点之一。
而要对有关物 质进行严格的控制,就离不开专属性强、灵敏度高的分析方法,这就涉及到分析方法的筛选 与验证。从现有的申报资料看,药品研发单位已基本上意识到分析方法验证的重要性,但是 对验证时各具体指标是否可行尚没有一个明确的可接受标准,从而难以对验证结果进行评 判。
为解决这一问题,本文结合国外一些大型药品研发企业在此方面的要求,提出了在对有 关物质检查方法进行验证时的可接受标准,供国内的药品研发单位在进行研究时参考。
1.准确度 该指标主要是通过回收率来反映。 验证时一般要求根据有关物质的定量限与质量标准中 该杂质的限度分别配制三个浓度的供试品溶液各三份(例如某杂质的限度为 0.
2%,则可分 别配制该杂质浓度为 0.1%、0.2%和 0.3%的杂质溶液),分别测定其含量,将实测值与理 论值比较,计算回收率,并计算 9 个回收率数据的相对标准差(RSD)。 该项目的可接受的标准为:各浓度下的平均回收率均应在 80%-120%之间,如杂质的浓度 为定量限,则该浓度下的平均回收率可放宽至 70%-130%,相对标准差应不大于 10%。
2.线性 线性一般通过线性回归方程的形式来表示。
具体的验证方法为: 在定量限至一定的浓度范围内配制 6 份浓度不同的供试液,分别测定该杂质峰的面积,计 算相应的含量。以含量为横坐标(X),峰面积为纵坐标(Y),进行线性回归分析。 可接受的标准为:回归线的相关系数(R)不得小于 0.
990,Y 轴截距应在 100%响应值的 25%以内,响应因子的相对标准差应不大于 10%。 3.精密度 1)重复性 配制 6 份杂质浓度(一般为 0.
1%)相同的供试品溶液,由一个分析人员在尽可能相同 的条件下进行测试,所得 6 份供试液含量的相对标准差应不大于 15%。 2)中间精密度 配制 6 份杂质浓度(一般为 0.1%)相同的供试品溶液,分别由两个分析人员使用不同 的仪器与试剂进行测试,所得 12 个含量数据的相对标准差应不大于 20%。
4.专属性 可接受的标准为:空白对照应无干扰,该杂质峰与其它峰应能完全分离,分离度不得小 于 2.
0。 5.检测限 杂质峰与噪音峰信号的强度比应不得小于 3。 6.定量限 杂质峰与噪音峰信号的强度比应不得小于 10。另外,配制 6 份最低定量限浓度的溶液, 所测 6 份溶液杂质峰保留时间的相对标准差应不大于 2.
0%,峰面积的相对标准差应不大于 5.0%。 7.耐用性 分别考察流动相比例变化± 5%、流动相 pH 值变化± 0.2、柱温变化± 5℃、检测波长变化 ± 5nm、流速相对值变化± 20%以及采用三根不同批号的色谱柱进行测定时,仪器色谱行为 的变化,每个条件下各测试两次。
可接受的标准为:各杂质峰的拖尾因子不得大于 2.0,杂 质峰与其他成分峰必须达到基线分离;各条件下的杂质含量数据(n=6)的相对标准差应不 大于 2.
0%,杂质含量的绝对值在± 0.1%以内。 8、系统适应性 配制 6 份相同浓度的杂质溶液进行分析, 该杂质峰峰面积的相对标准差应不大于 2.0%, 保留时间的相对标准差应不大于 1.
0%。另外,杂质峰的拖尾因子不得大于 2.0,理论塔板 数应符合质量标准的规定。 9.溶液稳定性 按照分析方法分别配置对照品溶液与供试品溶液,平行测定两次主成分与杂质的含量, 然后将上述溶液分别贮存在室温与冰箱冷藏室(4℃)中,在 1、2、3、5 和 7 天时分别平 行测定两次主成分与杂质的含量。
可接受的标准为:主成分的含量变化的绝对值应不大于 2.0%,杂质含量的绝对值在 ± 0.1%以内,并不得出现新的大于报告限度的杂质。