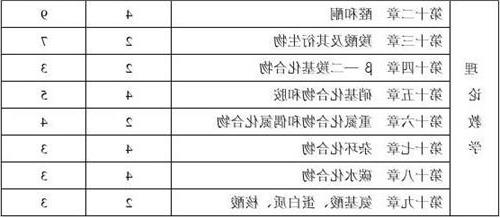
黄鸣龙反应机理 有机反应和反应机理总结83
1乌尔夫-凯惜纳-黄鸣龙还原:将醛或酮、肼和氢氧化钾在一高沸点的溶剂如一缩二乙二醇(HOCH2CH2OCH2CH2OH,沸点245˚C)中进行反应,使醛或酮的羰基被还原成亚甲基,这个方法称为乌尔夫-凯惜纳(Wolff
L−Kishner N M)-黄鸣龙方法还原。对酸不稳定而对碱稳定的羰基化合物可以用此法还原。
2去氨基还原:重氮盐在某些还原剂的作用下,能发生重氮基被氢原子取代的反应,由于重氮基来自氨基,因此常称该反应为去氨基还原反应。
3异相催化氢化:适用于烯烃氢化的催化剂有铂、钯、铑、钌、镍等,这些分散的金属态的催化剂均不溶于有机溶剂,一般称之为异相催化剂。在异相催化剂作用下发生的加氢反应称为异相催化氢化。
4麦尔外因—彭杜尔夫还原:醛酮用异丙醇铝还原成醇的一种方法。这个反应一般是在苯或甲苯溶液中进行。异丙醇铝把氢负离子转移给醛或酮,而自身氧化成丙酮,随着反应进行,把丙酮蒸出来,使反应朝产物方面进行。这是欧芬脑尔氧化法的逆反应,叫做麦尔外因—彭杜尔夫(Meerwein H-Ponndorf W)反应。
5卤代烃的还原:卤代烃被还原剂还原成烃的反应称为卤代烃的还原。还原试剂很多,目前使用较为普遍的是氢化锂铝,它是个很强的还原剂,所有类型的卤代烃包括乙烯型卤代烃均可被还原,还原反应一般在乙醚或四氢呋喃(THF)等溶剂中进行。
6伯奇还原:碱金属在液氨和醇的混合液中,与芳香化合物反应,苯环被还原为1,4-环己二烯类化合物,这种反应被称为伯奇还原。
7均相催化氢化:一些可溶于有机溶剂中的催化剂称为均相催化剂。在均相催化剂作用下发生的加氢反应称为均相催化氢化。
8克莱门森还原:醛或酮与锌汞齐和浓盐酸一起回流反应。醛或酮的羰基被还原成亚甲基,这个方法称为克莱门森还原。
9罗森孟还原法:用部分失活的钯催化剂使酰氯进行催化还原生成醛。此还原法称为罗森孟(Posenmund, K. W.)还原法。
10斯蒂芬还原:将氯化亚锡悬浮在乙醚溶液中,并用氯化氢气体饱和,将芳腈加入反应,水解后得到芳醛。此还原法称为斯蒂芬(Stephen, H.)还原。 11催化氢化:在催化剂的作用下,不饱和化合物与氢发生的加氢反应称之为催化氢化。
12催化氢解:用催化氢化法使碳与杂原子(O,N,X等)之间的键断裂,称为催化氢解。苯甲位的碳与杂原子之间的键很易催化氢解。
13酮的双分子还原:在钠、铝、镁、铝汞齐或低价钛试剂的催化下,酮在非质子溶剂中发生双分子还原偶联生成频哪醇,该反应称为酮的双分子还原。 14硼氢化-还原反应:烯烃与甲硼烷作用生成烷基硼的反应称为烯烃的硼氢化反
应。烷基硼和羧酸作用生成烷烃的反应称为烷基硼的还原反应。该反应与烯烃的硼氢化反应合在一起,总称为硼氢化-还原反应。
15鲍维特—勃朗克还原:用金属钠-醇还原酯得一级醇,称为鲍维特—勃朗克(Bouveault –Blanc)还原。
16醛酮用活泼金属的单分子还原:用活泼金属如钠、铝、镁和酸、碱、水、醇等作用,可以顺利地将醛还原为一级醇、将酮还原为二级醇。这是醛酮用活泼金属的单分子还原。
(6)缩合反应
1达参反应:醛或酮在强碱(如醇钠、氨基钠等)的作用下和一个a-卤代羧酸酯反应,生成a,b-环氧酸酯的反应称为达参(Darzen, G.)反应。
2安息香缩合反应:苯甲醛在氰离子(CN—)的催化作用下,发生双分子缩合生成安息香,因此称此反应为安息香缩合反应。很多芳香醛也能发生这类反应, 3狄克曼反应:二元酸酯可以发生分子内的及分子间的酯缩合反应。
假若分子中的两个酯基被四个或四个以上的碳原子隔开时,就发生分子内的缩合反应,形成五元环或更大环的酯,这种环化酯缩合反应又称为狄克曼(Dieckmann)反应。 4脑文格反应:在弱碱的催化作用下,醛、酮和含有活泼亚甲基的化合物发生的失水缩合反应称为脑文格(knoevenagel)反应。
5浦尔金反应:在碱性催化剂的作用下,芳香醛与酸酐反应生成b-芳基-a,b-不饱和酸的反应称为浦尔金(Perkin)反应。所用的碱性催化剂通常是与酸酐相对应的羧酸盐。
6曼尼希反应:具有活泼氢的化合物、甲醛、胺同时缩合,活泼氢被胺甲基或取代胺甲基代替的反应称为胺甲基化反应,也称为曼尼希(Mannich)反应,简称曼氏反应。
7羟醛缩合反应:有a-氢的醛或酮在酸或碱的催化作用下,缩合形成b-羟基醛或b-羟基酮的反应称为羟醛缩合反应。
8鲁宾逊增环反应:环己酮及其衍生物在碱(如氨基钠、醇钠等)存在下,与曼氏碱的季铵盐作用产生二并六元环的反应称为鲁宾逊(Robinson)增环反应。 9瑞佛马斯基反应:醛和酮与a-溴代酸酯和锌在惰性溶剂中相互作用得到b-羟基酸酯的反应称为瑞佛马斯基(Reformatsky)反应。
10酯缩合反应(克莱森缩合反应):两分子酯在碱的作用下失去一分子醇生成b-羰基酯的反应称为酯缩合反应,也称为克莱森缩合反应。
11酮醇缩合:脂肪酸酯和金属钠在乙醚或甲苯、二甲苯中,在纯氮气流存在下(微量氧的存在会降低产量)剧烈搅拌和回流,发生双分子还原,得a-羟基酮(也叫酮醇),此反应称为酮醇缩合(acyloin condensation)。
12魏悌息反应:魏悌息(Wittig,G.)试剂可以和酮或醛的羰基进行亲核加成,最后形成烯烃,这个反应称为魏悌息反应。
13魏悌息-霍纳尔反应:魏悌息-霍纳尔试剂很容易与醛酮反应生成烯烃,该反应称为魏悌息-霍纳尔(Witting-Horner)反应。
(7)重排反应
1二苯乙醇酸重排:二苯乙二酮在~70%氢氧化钠溶液中加热,重排成二苯乙醇酸的反应称为二苯乙醇酸重排。
2贝克曼重排:酮肟在酸性催化剂如硫酸、多聚磷酸以及能产生强酸的五氯化磷、
三氯化磷、苯磺酰氯、亚硫酰氯等作用下重排成酰胺的反应称为贝克曼重排。 3弗里斯重排:酚酯与路易斯酸一起加热,可发生酰基重排,生成邻羟基和对羟基芳酮的混和物,此反应称为弗里斯(Fries)重排。
4异丙苯的氧化重排:该法以丙烯和苯为起始原料,首先苯和丙烯在三氯化铝的作用下,产生异丙苯,异丙苯三级碳原子上的氢比较活泼,在空气的直接作用下,氧化成过氧化物,过氧化物在酸的作用下,失去一分子水,形成一个氧正离子,苯环带着一对电子转移到氧上,发生所谓的缺少电子的氧所引起的重排反应,得到―碳正‖离子,―碳正‖离子再和水结合,去质子分解成丙酮及苯酚。上述过程称为异丙苯的氧化重排。
5克尔提斯反应:由酰氯和叠氮化合物制备酰基叠氮,酰基叠氮在惰性溶剂中加热分解,失去氮气后,重排成异氰酸酯,然后水解得一级胺。这个反应称为克尔提斯(Cartius)反应。
6克莱森重排:克莱森(Claisen) 发现:烯丙基芳基醚在高温(200°C)可以重排为邻烯丙基酚,这称为邻位克莱森重排。邻烯丙基酚可以再进一步重排得到对烯丙基酚,这称为对位克莱森重排。上述重排统称为克莱森重排。
7阿恩特—艾司特反应:重氮甲烷与酰氯反应首先形成重氮酮,重氮酮在氧化银催化下与水共热,得到酰基卡宾,酰基卡宾发生重排得烯酮,烯酮与水反应产生酸;如果用醇或氨(胺)代替水,则得酯或酰胺。此反应称阿恩特(Arndt)—艾司特(Eistert)反应。
8法沃斯基重排反应:在醇钠、氢氧化钠、氨基钠等碱性催化剂存在下,α−卤代酮(α−氯代酮或α−溴代酮)失去卤原子,重排成具有相同碳原子数的羧酸酯、羧酸、酰胺的反应称为法沃斯基重排。
-碳之间的键断裂,插入一个氧形成酯的反应称为拜尔(Boeyer)-魏立格(Villiger V)氧化重排:a9拜尔-魏立格氧化重排:酮类化合物被过酸氧化,羰基碳与 10施密特反应:将羧酸与等物质的量的叠氮酸(HN3)在惰性溶剂中用硫酸作缩合剂进行缩合。然后在无机酸的作用下,使酰基叠氮分解,重排,最后水解为一级胺。这个反应称为施密特 (Schmitt)反应。
11瓦格奈尔-梅尔外英重排:一个不稳定的碳正离子会重排为一个更稳定的碳正离子,当醇羟基与三级碳原子或二级碳原子相连时,在酸催化的脱水反应中,常常会发生此类重排反应,称为瓦格奈尔(Wagner, G.)-梅尔外英(Meerwein, H.)重排。
12蒂芬欧-捷姆扬诺夫反应:1-氨甲基环烷醇与亚硝酸反应得到环增大一个碳的环酮。该反应称为蒂芬欧(Tiffeneau)-捷姆扬诺夫 (Demjanov)反应。 13联苯胺重排:氢化偶氮苯在酸催化下发生重排,生成4,4’-二氨基联苯的反应称为联苯胺重排。
对位被取代的氢化偶氮苯重排时,重排一般在邻位发生。 14频哪醇重排:邻二醇在酸作用下发生重排生成酮的反应。这类反应最初是从频哪醇重排为频哪酮发现的,因此被称为频哪醇重排反应。
反应过程如下:首先羟基质子化,然后失水形成碳正离子,相继发生基团的迁移,缺电子中心转移到羟基的氧原子上,再失去质子生成频哪酮。α−双二级醇,α−二级醇三级醇、α−双三级醇均能发生此反应。
15霍夫曼重排反应:酰胺与次卤酸盐(工业上常用NaOCl,实验室中常用NaOBr)的碱溶液(或卤素的氢氧化钠溶液)作用时,放出二氧化碳,生成比酰胺少一个碳原子的一级胺的反应称为霍夫曼 (Hofmann)重排反应,也称霍夫曼 (Hofmann)降解反应。
(8)周环反应
1电环化反应:在光或热的作用下,共轭烯烃末端两个碳原子的π电子环合成一个σ键,从而形成比原来分子少一个双键的环烯烃或它的逆反应——环烯烃开环变为共轭烯烃,这类反应统称为电环化反应。
2 σ-迁移反应:在化学反应中,一个σ键沿着共轭体系由一个位置转移到另一个位置,同时伴随着π键转移的反应称为σ-迁移反应。在σ-迁移反应中,原有σ键的断裂,新σ键的形成以及π键的迁移都是经过环状过渡态协同一步完成的。
3狄尔斯−阿尔德反应:1928年,德国化学家狄尔斯(Diels, O.)和阿尔德(Alder, K.)在研究1,3−丁二烯和顺丁烯二酸酐的互相作用时发现了一类反应——共轭双烯与含有烯键或炔键的化合物互相作用,生成六元环状化合物的反应。
这类反应称为狄尔斯−阿尔德(Diels−Alder)反应。又称双烯合成。
狄尔斯−阿尔德反应分为三类:将电子从双烯体的HOMO流入亲双烯体的LUMO的反应称为正常的D-A反应;将电子从亲双烯体的HOMO流入双烯体的LUMO的反应称为反常的D-A反应;电子双向流动的反应称为中间的D-A反应。
4环加成反应:在光或热的作用下,两个或多个带有双键、共轭双键或孤对电子的分子相互作用,形成一个稳定的环状化合物的反应称为环加成反应。环加成反应的逆反应称为环消除反应。
5周环反应:在化学反应过程中,能形成环状过渡态的协同反应统称为周环反应。
(9)其它
1刘卡特反应:醛或酮在高温下与甲酸铵反应得一级胺,这个反应称为刘卡特(Leuckart)反应。首先甲酸铵受热分解为氨和甲酸,氨和醛或酮反应生成亚胺,甲酸作为还原剂先提供一个正氢再提供一个负氢将亚胺还原成胺。
2兴斯堡反应:一级胺、二级胺、三级胺与磺酰氯的反应称为兴斯堡(Hinsberg)反应。兴斯堡反应可以在碱性条件下进行,一级胺反应产生的磺酰胺,氮上还有一个氢,因受磺酰基影响,具有弱酸性,可以溶于碱成盐;二级胺形成的磺酰胺因氮上无氢,不溶于碱;三级胺虽然能与磺酰氯反应生成 ,但被水分解又回到原来的三级胺,因此可以认为不发生这个反应。
不起兴斯堡反应的三级胺,可溶于酸,因此利用这个反应可区别一级胺、二级胺和三级胺。也可以利用生成的磺酰胺性质上的不同,用来分离与鉴定三类胺。
3卤仿反应:甲基酮类化合物或能被次卤酸钠氧化成甲基酮的化合物,在碱性条件下与氯、溴、碘作用分别生成氯仿、溴仿、碘仿(统称卤仿)的反应称为卤仿反应。
4质子化反应:分子接受一个质子的反应称为质子化反应。
5卤仿的分解反应:氯仿遇空气或日光会分解成剧毒的光气,此反应称为卤仿的分解反应。
6埃斯韦勒—克拉克甲基化反应:在过量甲酸的存在下,甲醛与一级胺或二级胺反应生成甲基化的三级胺,此反应称为埃斯韦勒(Eschweiler)—克拉克(Clarke)甲基化反应。甲醛在反应中可以当作一个甲基化试剂。
7烯烃的羟汞化-去汞还原反应:醋酸汞水溶液和烯烃经环汞化、反式开环生成-羟基有机汞化合物的反应称为烯烃的羟汞化。该有机汞化合物与硼氢化钠反应,化合物中的碳汞键(C−Hg)被还原为碳氢键(C−H)。
烯烃的羟汞化和相应有机汞化合物的还原统称为烯烃的羟汞化-去汞还原反应。 8烯烃的烷氧汞化——去汞还原反应:醋酸汞醇溶液和烯烃经环汞化、反式开环生成-烷氧基有机汞化合物的反应称为烯烃的烷氧汞化反应。
该有机汞化合物与硼氢化钠反应,金属化合物中的碳汞键(C−Hg)被还原为碳氢键(C−H)。烯烃的烷氧汞化和有机汞化合物的还原统称为烯烃的烷氧汞化-去汞还原反应。
9酮式分解:乙酰乙酸乙酯在稀的碱溶液中水解,再酸化,生成乙酰乙酸,稍加热失羧,生成丙酮。因此将乙酰乙酸乙酯在稀碱中水解、再失羧称为酮式分解。酮式分解的概念也适用于其它酮酯或b-二酯化合物。即任何酮酯或b-二酯化合物经在稀碱中水解,然后酸化、加热失羧的反应都称为酮式分解。取代的乙酰乙酸乙酯经酮式分解得到丙酮的衍生物。
10酸式分解:用浓的强碱溶液和乙酰乙酸乙酯同时加热,再酸化,得到的主要产物是两个酸,所以叫做酸式分解。酸式分解的概念也适用于其它酮酯或b-二酯化合物,即酮酯或b-二酯化合物在浓的强碱溶液中发生羰基碳和亚甲基碳之间的断裂的反应都属于酸式分解。取代的乙酰乙酸乙酯和取代的丙二酸二乙酯经酸式分解都得到乙酸的衍生物。丙二酸二乙酯经酸式分解得乙酸。
11醛或酮的还原氨(胺)化:氨或胺可以与醛或酮缩合,得亚胺,如存在氢及催化剂或氢化试剂,立即还原为相应的一级、二级或三级胺,这个方法称为醛或酮的还原氨(胺)化。
(10)合成法
1毕歇尔—钠皮尔拉斯基合成法:是合成1-取代异喹啉化合物最常用的方法。 首先用苯乙胺与羧酸或酰氯反应,形成酰胺,然后在失水剂如五氧化二磷、三氯氧磷或五氯化磷等作用下,失水关环,再脱氢得1-取代异喹啉化合物。
2佑尔业夫法:以氧化铝为催化剂,分别以NH3、H2O、H2S为试剂,使吡咯、呋喃和噻吩的环系互变。此法称为佑尔业夫(Yure’v.)法。