施一公课题组 施一公教授课题组《科学》杂志连发两篇重要突破
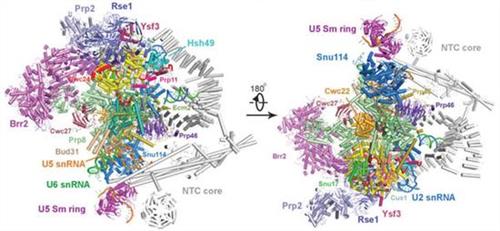
剪接体是一类大型复合物,能将RNA中的内含子模板移除,并将外显子序列连接起来。2015年,中国科学院院士施一公教授领导的团队在《科学》杂志上“背靠背”刊登两篇重磅论文,首次获取了真核细胞剪接体复合物的高分辨率三维结构,并详细阐述了剪接体对前体mRNA进行剪接的基本作用机理。
施一公教授曾表示“这项成果的重要性超过我过去25年科学研究总和”。而在昨日出版的《科学》杂志上,施一公教授的课题组再次发表两篇关于剪接体的重量级论文,进一步阐明了这一关键复合体的详细作用机制。我们对这一成就表示祝贺!
众所周知,mRNA剪接是蛋白质翻译过程中必需步骤。从染色体DNA上转录出来的前体mRNA(pre-mRNA)并不直接参与蛋白质翻译,而是需要先将其中的内含子片段切除,才能进入蛋白质的翻译场所——核糖体。
这当中的内含子剪接过程需分轮进行,每一轮会通过两步反应切除一段内含子区域。其中,第一步由位于待切除内含子3’端区域、具有高度保守性的分支点序列(BPS)中的特定腺嘌呤(A)核苷酸介导,该核苷酸的2’-羟基对位于内含子5’端第一个核苷酸的剪接位点(5’SS)发起双分子亲核取代反应(SN2),形成套索(lariat)中间体结构。
之后,由此释放的原来位于内含子5’端外显子片段的3’-羟基又会向内含子3’端最后一个核苷酸的剪接位点发动亲核攻击,通过SN2反应与原来位于内含子3’端外显子片段连接起来,同时释放掉内含子套索结构。