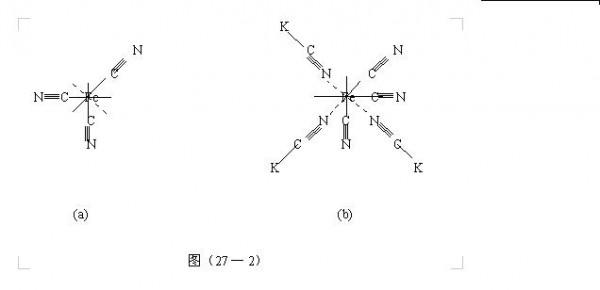
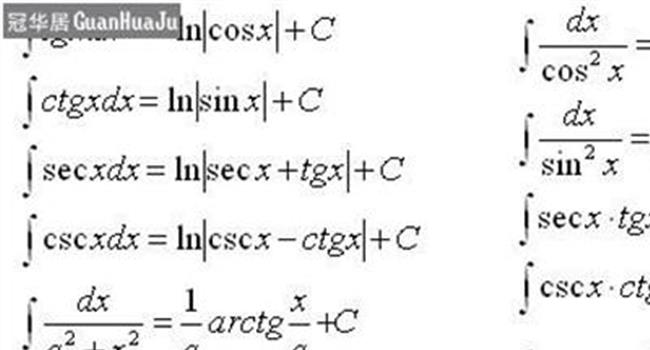索末菲椭圆轨道理论
玻尔原来的理论仅考虑氢原子中电子绕核作圆轨道运动,索末菲推广考虑了椭圆轨道。平面椭圆轨道有两个自由度,需要两个量子化条件,空间椭圆轨道则需要3个量子化条件 。 索末菲采用推广了的玻尔量子化条件 ,得出氢原子系统的能量是量子化的 , 仍由主量子数n确定 ,与玻尔理论结果相同,而氢原子的角动量由角量子数确定 ,相同主量子数不同椭圆轨道上的角动量不同,且是量子化的,椭圆形状也是量子化的;在三维情形下,椭圆轨道以及角动量的空间取向也是量子化的。
索末菲还进而考虑电子在椭圆轨道上运动速度变化引起的相对效应,得出氢原子能级的精细结构,与实验结果相符。
索末菲理论属于前期量子论,其中仍保留了电子运动轨道的概念,不同于后来发展起来的量子力学概念,而且某些结果的细节也与实际不符。
索末菲椭圆轨道理论计算方法编辑
(图1)A.索末菲在玻尔氢原子理论的圆轨道基础上发展了椭圆轨道理论,认为电子在核的库仑场中运动,其轨道一般应为椭圆。索末菲假定在极坐标系中电子的允许轨道必须满足两个量子条件(图1) ,
(图2)式中n嗞和nr都是正整数,分别称为角量子数和径量子数。核库仑吸引力是一种有心力,故电子的角动量p嗞在周期运动中为恒量(图2)。
(图3)利用这一关系,再用经典力学中粒子作椭圆轨道运动时总能量关系,算得氢原子中电子在椭圆轨道上的总能量为(图3),式中me是电子的质量,Z是原子核电荷数,e是电子的电荷量,ε0是真空介电常数, h是普朗克常数。如果令n
(图4)=nr n嗞,则电子在椭圆轨道上的能量与相应的玻尔轨道上的能量相同。整数 n称为主量子数。并且算得椭圆轨道的半长轴a为(图4)。半长轴a和半短轴b的关系为(图5) (图5)。 对每一个半长轴,都有n个不同半短轴的轨道,按开普勒定律,作椭圆轨道运动粒子的能量只和长轴有关,故这些轨道上的电子具有相同的能量(图6), (图6)En只与n有关, (图7)与n嗞无关。
考虑到电子质量的相对论效应,在偏心率不同的轨道上的影响是不同的,索末菲详细推导了相对论效应中电子能量,得到(图7),式中μ为电子与核的静折 (图8)合质量,R为该原子的里德伯常数,с为真空中光速(图8),
称为精细结构常数。可见,相对论效应使得主量子数n相同,但角量
子数n嗞不同的椭圆轨道具有不同的能量,即同一个n值所标示的能级将分裂为n个相近的能级。据此也能解释光谱的精细结构。 (图10)1926年L.H.托马斯首先根据G.E.乌伦贝克电子自旋的假设,考虑到自旋轨道相互作用和相对论坐标变换效应,成功地解释了氢原子光谱精细结构谱线分裂。
1927年P.A.M.狄喇克的相对论量子力学理论直接得到了 (图9)相似的结果(图9)(图10),式中j取值和(l-1/2),称总角动量量子数。狄喇克理论不仅能较好地定量解释氢原子光谱的精细结构,而且可直接导出电子的自旋磁矩。